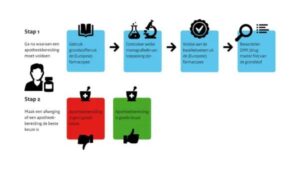
Uitdagingen in de farmaceutische productie
De productie van werkzame stoffen moet voldoen aan de GMP-richtlijnen (deel II) [1]. Voor geregistreerde producten en magistrale bereidingen, is de gekwalificeerde persoon (QP), die het eindproduct vrijgeeft, ook verantwoordelijk voor het waarborgen dat de gebruikte werkzame stoffen conform deze richtlijnen zijn geproduceerd.
EU-wetgeving
Volgens de EU-wetgeving moet elke levering van werkzame stoffen uit landen buiten de EU worden begeleid door een verklaring van de autoriteiten van dat land [2]. Hierin moet staan dat de stof is vervaardigd volgens de Europese GMP-normen (een ‘schriftelijke bevestiging’ ofwel een ‘Written Conformation’). ‘Derde landen’ zijn uitgezonderd als ze aantoonbaar een wetgevend kader hebben voor inspectie en handhaving van GMP-conforme productie van werkzame stoffen [3]. Deze landen staan op de zogenaamde White List en betreffen bijvoorbeeld Japan, de USA en Brazilië.
Ofipharma: Kwaliteitsborging in grondstofselectie
Ofipharma streeft naar een naadloze implementatie van deze kwaliteitsstandaarden in grootbereidingsfaciliteiten, openbare apotheken en ziekenhuisapotheken. De kwaliteitsbewaking bij Ofipharma is zodoende uitmuntend te noemen. Het achterhalen van de oorsprong van grondstoffen, vooral die uit landen zoals China of India, is een complexiteit waar individuele apothekers vaak mee worstelen. Wij staan garant voor een grondige evaluatie van de producenten en wij bieden uitsluitend grondstoffen die afkomstig zijn van goedgekeurde producenten. Indien dit niet het geval is, zal Ofipharma verzoeken om een schriftelijke verklaring (spot declaration) van de apotheek. Bovendien biedt Ofipharma ondersteuning bij het vinden, beoordelen en analyseren van grondstoffen. Dit resulteert in hoogwaardige materialen vergezeld van de juiste documentatie.
Risicobeoordeling
Niettemin is soms een risicobeoordeling nodig om het evenwicht te vinden tussen het voordeel van het leveren van een product aan een patiënt en het niveau van GMP-naleving van de grondstof. Dit vereist een afweging van de klinische gevolgen van het niet leveren van het product en de kennis over de productie- en toeleveringsketen van de grondstof, en in hoeverre deze voldoen aan de EU GMP-normen.
Problemen met onvoldoende gecontroleerde grondstoffen
Een voorbeeld van problemen met onvoldoende gecontroleerde grondstoffen deed zich voor in China met heparine, dat vermengd was met een schadelijke stof. Dit resulteerde in ernstige reacties bij patiënten in de VS door vervuilde medicijnen. De Europese Farmacopee heeft haar richtlijnen aangepast om dergelijke onzuiverheden te detecteren [4]. In 2013 heeft de FDA richtlijnen uitgegeven aan fabrikanten om de heparine-toeleveringsketen te beschermen tegen dergelijke besmettingen [5].
Voldoende na volledige heranalyse
In 2023 heeft de IGJ (Inspectie Gezondheidszorg en Jeugd) de heparine van Ofipharma beoordeeld tijdens de GMP-inspectie. Alle aspecten van de beoordeling van de fabrikant tot aan de vrijgave na een volledige heranalyse volgens de Europese Farmacopee (EP) zijn als voldoende beoordeeld. Hier zijn wij trots op!
Gebruikte bronnen in dit artikel
- Anonymous, Eudralex – Volume 4 – Good Manufacturing Practice (GMP) guidelines. https://ec.europa.eu/health/documents/eudralex/vol-4_en. Accessed 29 November 2021
- Falsified Medicines Directive 2011/62/EU of the European Parliament and of the Council of 8 June 2011, L174/74, Official Journal of the European Union 1 Jun 2011
- European Commission, Importation of active substances – Listing of third countries. https://ec.europa.eu/health/international_cooperation/pharmaceuticals/Importation_activesubstances_en,. Assessed 29 November 2021
- EMA/CHMP/278280/2008 Assessment report for medicinal products containing or derived from heparin, May 2008
- U.S. FDA Guidance for Industry. Heparin for Drug and Medical Device Use: Monitoring Crude Heparin for Quality, June 2013
Heeft u vragen of wilt u meer informatie over de dienstverlening van Ofipharma?